categorieën: Aanbevolen artikelen » Interessant elektrisch nieuws
Aantal keer bekeken: 51203
Reacties op het artikel: 7
Wat zijn brandstofcellen
 Mobiele elektronica wordt elk jaar, zo niet een maand, steeds toegankelijker en wijdverbreid. Hier heb je laptops en PDA's en digitale camera's en mobiele telefoons, en een heleboel allerlei handige en niet zo apparaten. En al deze apparaten krijgen continu nieuwe functies, krachtigere processors, grote kleurenschermen, draadloze communicatie, terwijl ze tegelijkertijd kleiner worden. Maar in tegenstelling tot halfgeleidertechnologieën gaan de energietechnologieën van al deze mobiele menagerie niet met grote sprongen vooruit.
Mobiele elektronica wordt elk jaar, zo niet een maand, steeds toegankelijker en wijdverbreid. Hier heb je laptops en PDA's en digitale camera's en mobiele telefoons, en een heleboel allerlei handige en niet zo apparaten. En al deze apparaten krijgen continu nieuwe functies, krachtigere processors, grote kleurenschermen, draadloze communicatie, terwijl ze tegelijkertijd kleiner worden. Maar in tegenstelling tot halfgeleidertechnologieën gaan de energietechnologieën van al deze mobiele menagerie niet met grote sprongen vooruit.
Conventionele oplaadbare batterijen en batterijen zijn duidelijk niet voldoende om de nieuwste ontwikkelingen in de elektronica-industrie voor een aanzienlijke hoeveelheid tijd aan te sturen. En zonder betrouwbare en ruime batterijen gaat het hele punt van mobiliteit en draadloosheid verloren. Dus de computerindustrie werkt steeds actiever aan het probleem alternatieve voedingen. En de meest veelbelovende vandaag is richting brandstofcellen.
Het basisprincipe van de werking van brandstofcellen werd ontdekt door de Britse wetenschapper Sir William Grove in 1839. Hij staat bekend als de vader van de brandstofcel. William Grove produceerde elektriciteit door te veranderen elektrolyse van water om waterstof en zuurstof te extraheren. Nadat hij de batterij van de elektrolytische cel had losgekoppeld, was Grove verrast dat de elektroden het vrijgekomen gas begonnen op te nemen en stroom te genereren. Proces opening elektrochemische koude verbranding van waterstof een gebeurtenis in de energiesector werd belangrijk en in de toekomst speelden bekende elektrochemici als Ostwald en Nernst een grote rol bij de ontwikkeling van de theoretische basis en de praktische implementatie van brandstofcellen en voorspelden een grote toekomst voor hen.
zichzelf de term "brandstofcel" (Fuel Cell) verscheen later - het werd in 1889 voorgesteld door Ludwig Mond en Charles Langer, die probeerden een apparaat te maken voor het opwekken van elektriciteit uit lucht en kolengas.
Tijdens normale verbranding oxideert zuurstof fossiele brandstoffen en wordt de chemische energie van de brandstof ineffectief omgezet in thermische energie. Maar het bleek mogelijk om de oxidatiereactie, bijvoorbeeld waterstof met zuurstof, in een elektrolytmedium en in aanwezigheid van elektroden uit te voeren om een elektrische stroom te verkrijgen. Als we bijvoorbeeld waterstof leveren aan een elektrode die zich in een alkalisch medium bevindt, verkrijgen we elektronen:
2H2 + 4OH- → 4H2O + 4e-
die, via het externe circuit, naar de tegenovergestelde elektrode gaan, waar zuurstof in komt en waar de reactie plaatsvindt: 4e- + O2 + 2H2O → 4OH-
Het is te zien dat de resulterende reactie 2H2 + O2 → H2O dezelfde is als tijdens normale verbranding, maar in de brandstofcel of anderszins in elektrochemische generator, het blijkt elektrische stroom met een hoog rendement en gedeeltelijk warmte. Merk op dat steenkool, koolmonoxide, alcoholen, hydrazine, andere organische stoffen kunnen ook worden gebruikt als brandstof in brandstofcellen en lucht, waterstofperoxide, chloor, broom, salpeterzuur, enz. kunnen worden gebruikt als oxidatiemiddelen.
De ontwikkeling van brandstofcellen ging krachtig door, zowel in het buitenland als in Rusland, en verder in de USSR. Onder de wetenschappers die een grote bijdrage hebben geleverd aan de studie van brandstofcellen, noemen we V. Zhako, P. Yablochkov, F. Bacon, E. Bauer, E. Justi, K. Cordes. In het midden van de vorige eeuw begon een nieuwe aanval op brandstofcelproblemen. Dit komt mede door de opkomst van nieuwe ideeën, materialen en technologieën als gevolg van defensieonderzoek.
Een van de wetenschappers die een belangrijke stap heeft gezet in de ontwikkeling van brandstofcellen was P. M. Spiridonov. Waterstof-zuurstofelementen van Spiridonov gaf een stroomdichtheid van 30 mA / cm2, wat voor die tijd als een geweldige prestatie werd beschouwd.In de jaren veertig creëerde O. Davtyan een installatie voor de elektrochemische verbranding van generatorgas verkregen door kolenvergassing. Met elke kubieke meter elementvolume ontving Davtyan 5 kW vermogen.
Dat was het eerste vaste elektrolytbrandstofcel. Het had een hoog rendement, maar na verloop van tijd werd de elektrolyt onbruikbaar en moest deze worden vervangen. Vervolgens creëerde Davtyan eind jaren vijftig een krachtige installatie die de tractor voortstuwde. In diezelfde jaren ontwierp en bouwde de Engelse ingenieur T. Bacon een brandstofcelbatterij met een totale capaciteit van 6 kW en een rendement van 80%, werkend op zuivere waterstof en zuurstof, maar de verhouding van vermogen tot batterijgewicht was te klein - dergelijke elementen waren ongeschikt voor praktisch gebruik en ook geliefden.
In de daaropvolgende jaren is de tijd van eenlingen voorbij. De makers van ruimtevaartuigen raakten geïnteresseerd in brandstofcellen. Sinds het midden van de jaren 60 is er miljoenen geïnvesteerd in onderzoek naar brandstofcellen. Het werk van duizenden wetenschappers en ingenieurs toegestaan om een nieuw niveau te bereiken, en in 1965. brandstofcellen werden getest in de Verenigde Staten op het ruimteschip Gemini 5, en later op Apollo-schepen voor vluchten naar de maan en in het kader van het Shuttle-programma.
In de USSR werden brandstofcellen ontwikkeld op NPO Kvant, ook voor gebruik in de ruimte. In die jaren verschenen al nieuwe materialen - vaste polymeerelektrolyten op basis van ionenuitwisselingsmembranen, nieuwe soorten katalysatoren, elektroden. En toch was de werkstroomdichtheid klein - in het bereik van 100-200 mA / cm2 en was het platinagehalte op de elektroden enkele g / cm2. Er waren veel problemen in verband met duurzaamheid, stabiliteit en beveiliging.
De volgende fase van snelle ontwikkeling van brandstofcellen begon in de jaren 90. vorige eeuw en gaat nu verder. Het wordt veroorzaakt door de behoefte aan nieuwe efficiënte energiebronnen enerzijds vanwege het wereldwijde milieuprobleem van de toenemende uitstoot van broeikasgassen door de verbranding van fossiele brandstoffen en anderzijds door de uitputting van dergelijke brandstoffen. Omdat water het eindproduct is van de verbranding van waterstof in een brandstofcel, worden ze beschouwd als de schoonste vanuit het oogpunt van milieueffecten. Het grootste probleem is alleen om een effectieve en goedkope manier te vinden om waterstof te produceren.
Miljarden financiële investeringen in de ontwikkeling van brandstofcellen en waterstofgeneratoren moeten leiden tot een technologische doorbraak en het gebruik ervan in het dagelijks leven mogelijk maken: in cellen van mobiele telefoons, in auto's, in energiecentrales. Reeds demonstreren automobiele reuzen zoals Ballard, Honda, Daimler Chrysler en General Motors auto's en bussen die op 50 kW brandstofcellen rijden. Een aantal bedrijven heeft zich ontwikkeld demonstratie-installaties voor vaste brandstof elektrolytbrandstofcellen tot 500 kW. Maar ondanks een belangrijke doorbraak in het verbeteren van de prestaties van brandstofcellen, moeten nog veel problemen worden opgelost met betrekking tot hun kosten, betrouwbaarheid en veiligheid.
In tegenstelling tot batterijen en accu's worden in een brandstofcel zowel brandstof als oxidatiemiddel van buitenaf toegevoerd. De brandstofcel is slechts een bemiddelaar in de reactie en onder ideale omstandigheden zou het bijna voor altijd kunnen werken. Het mooie van deze technologie is dat in feite wordt brandstof in het element verbrand en wordt de vrijgekomen energie direct omgezet in elektriciteit. Bij directe verbranding van brandstof wordt het geoxideerd door zuurstof en de warmte die in dit proces wordt gegenereerd, wordt gebruikt om nuttig werk te voltooien.
In een brandstofcel worden, net als in batterijen, de reacties van brandstofoxidatie en zuurstofreductie ruimtelijk gescheiden en het proces van "branden" verloopt alleen als de cel stroom aan de lading afgeeft. Het is alsof dieselgenerator, alleen zonder diesel en generator. En ook zonder rook, lawaai, oververhitting en met veel hogere efficiëntie. Dit laatste wordt verklaard door het feit dat er ten eerste geen tussenliggende mechanische apparaten zijn en ten tweede dat de brandstofcel geen warmtemotor is en daarom niet voldoet aan de Carnot-wet (dat wil zeggen dat de efficiëntie ervan niet wordt bepaald door het temperatuurverschil).
Zuurstof wordt gebruikt als oxidatiemiddel in brandstofcellen. Aangezien zuurstof bovendien voldoende in de lucht aanwezig is, hoeft u zich geen zorgen te maken over de toevoer van een oxidatiemiddel. Wat brandstof betreft, het is waterstof. De reactie vindt dus plaats in de brandstofcel:
2H2 + O2 → 2H2O + elektriciteit + warmte.
Het resultaat is nuttige energie en waterdamp. De eenvoudigste in zijn ontwerp is protonuitwisselingsmembraan brandstofcel (zie figuur 1). Het werkt als volgt: de waterstof die het element binnenkomt ontleedt onder invloed van de katalysator in elektronen en positief geladen waterstofionen H +. Dan komt een speciaal membraan in het spel, dat hier werkt als een elektrolyt in een conventionele batterij. Vanwege zijn chemische samenstelling passeert het protonen door zichzelf, maar vangt het elektronen op. De elektronen die zich ophopen op de anode creëren dus een overmatige negatieve lading en waterstofionen creëren een positieve lading op de kathode (de spanning op het element is ongeveer 1V).
Om een hoog vermogen te creëren, wordt een brandstofcel samengesteld uit meerdere cellen. Als je een element in de belasting opneemt, stromen de elektronen erdoorheen naar de kathode, waardoor een stroom ontstaat en het proces van waterstofoxidatie door zuurstof wordt voltooid. Als katalysator in dergelijke brandstofcellen worden typisch platinamicrodeeltjes die zijn afgezet op een koolstofvezel gebruikt. Vanwege zijn structuur laat een dergelijke katalysator gas en elektriciteit goed door. Het membraan is typisch gemaakt van een zwavelhoudend Nafion-polymeer. De dikte van het membraan is gelijk aan tienden van een millimeter. Tijdens de reactie komt natuurlijk ook warmte vrij, maar dit is niet zo zeer, zodat de bedrijfstemperatuur binnen het bereik van 40-80 ° C wordt gehouden.
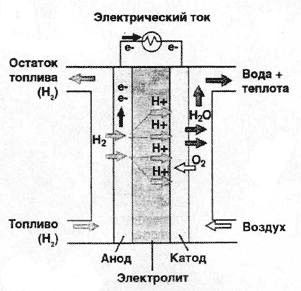
Afb.1. Het werkingsprincipe van de brandstofcel
Er zijn andere soorten brandstofcellen, voornamelijk verschillend in het type elektrolyt dat wordt gebruikt. Bijna allemaal hebben ze waterstof nodig als brandstof, dus een logische vraag rijst: waar kan ik het krijgen? Het zou natuurlijk mogelijk zijn om gecomprimeerde waterstof uit cilinders te gebruiken, maar dan zijn er onmiddellijk problemen bij het transport en de opslag van dit licht ontvlambare gas onder hoge druk. Natuurlijk kunt u waterstof in gebonden vorm gebruiken zoals in metaalhydride-batterijen. Maar toch blijft de taak van de winning en het transport, omdat de infrastructuur van waterstofgasstations niet bestaat.
Er is echter ook een oplossing - vloeibare koolwaterstofbrandstof kan worden gebruikt als een bron van waterstof. Bijvoorbeeld ethyl- of methylalcohol. Toegegeven, hier is al een speciaal extra apparaat vereist - een brandstofconvertor, die alcoholen bij hoge temperatuur omzet in een mengsel van gasvormig H2 en CO2 (voor methanol zal dit ergens rond de 240 ° C zijn). Maar in dit geval is het al moeilijker om na te denken over draagbaarheid - dergelijke apparaten worden goed gebruikt als stationaire of auto alternatorenMaar voor compacte mobiele apparatuur heb je iets minder omslachtigs nodig.
En hier komen we bij dat apparaat, de ontwikkeling waarvan bijna alle grootste fabrikanten van elektronica met vreselijke kracht bezig zijn - methanol brandstofcel (figuur 2).
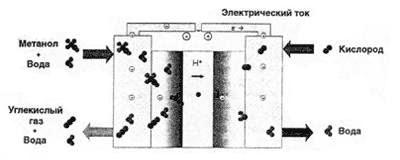
Afb.2. Het werkingsprincipe van de brandstofcel op methanol
Het fundamentele verschil tussen waterstof- en methanolvulelementen is de gebruikte katalysator. Met de katalysator in de methanolbrandstofcel kunnen protonen direct uit het alcoholmolecuul worden verwijderd.Het probleem van brandstof wordt dus opgelost - methylalcohol wordt in massa geproduceerd voor de chemische industrie, het is gemakkelijk op te slaan en te transporteren, en om een methanolbrandstofcel op te laden, is het voldoende om de cartridge eenvoudig door brandstof te vervangen. Toegegeven, er is een belangrijk minpunt: methanol is giftig. Bovendien is de efficiëntie van een methanolbrandstofcel aanzienlijk lager dan die van een waterstof.

Fig. 3. Methanol brandstofcel
De meest verleidelijke optie is om ethylalcohol als brandstof te gebruiken, omdat de productie en distributie van alcoholische dranken van elke samenstelling en sterkte over de hele wereld goed is ingeburgerd. De efficiëntie van ethanolbrandstofcellen is helaas zelfs lager dan die van methanol.
Zoals reeds opgemerkt gedurende vele jaren van ontwikkeling op het gebied van brandstofcellen, zijn verschillende soorten brandstofcellen gebouwd. Brandstofcellen worden ingedeeld per elektrolyt en type brandstof.
1. Vast polymeer waterstof-zuurstof elektrolyt.
2. Brandstofcellen van vaste polymere methanol.
3. Elementen op alkalische elektrolyt.
4. Fosforzuurbrandstofcellen.
5. Brandstofcellen op gesmolten carbonaten.
6. Vaste oxide brandstofcellen.
In het ideale geval is de efficiëntie van brandstofcellen zeer hoog, maar in reële omstandigheden zijn er verliezen verbonden aan niet-evenwichtsprocessen, zoals ohmse verliezen als gevolg van de geleidbaarheid van de elektrolyt en elektroden, activering en concentratiepolarisatie, diffusieverliezen. Hierdoor wordt een deel van de in de brandstofcellen opgewekte energie omgezet in warmte. De inspanningen van specialisten zijn gericht op het verminderen van deze verliezen.
De belangrijkste bron van ohmse verliezen, evenals de reden voor de hoge prijs van brandstofcellen, zijn geperfluoreerde sulfocatie-ionenuitwisselingsmembranen. Nu zijn ze op zoek naar alternatieve, goedkopere protongeleidende polymeren. Omdat de geleidbaarheid van deze membranen (vaste elektrolyten) alleen in aanwezigheid van water een acceptabele waarde (10 Ohm / cm) bereikt, moeten de aan de brandstofcel toegevoerde gassen extra worden bevochtigd in een speciaal apparaat, wat het systeem ook duurder maakt. In katalytische gasdiffusie-elektroden worden hoofdzakelijk platina en enkele andere edelmetalen gebruikt en tot nu toe is geen vervanging gevonden. Hoewel het platinagehalte in de brandstofcellen enkele mg / cm2 is, bereikt het voor grote batterijen tientallen grammen.
Bij het ontwerpen van brandstofcellen wordt veel aandacht besteed aan het warmteafvoersysteem, omdat het systeem bij hoge stroomdichtheden (tot 1A / cm2) zelf opwarmt. Voor koeling wordt water gebruikt dat door speciale kanalen in de brandstofcel circuleert en bij lage capaciteiten wordt lucht geblazen.
Dus, het moderne systeem van de elektrochemische generator, naast de brandstofcelbatterij zelf, "groeit" met vele hulpapparaten, zoals: pompen, compressor voor luchttoevoer, waterstofinlaat, gasbevochtiger, koelunit, gaslekcontrolesysteem, DC naar AC-omzetter, besturingsprocessor en anderen. Dit alles leidt ertoe dat de kosten van het brandstofcelsysteem in 2004-2005 2-3 duizend $ / kW waren. Volgens deskundigen zullen brandstofcellen beschikbaar komen voor gebruik in transport en in stationaire energiecentrales tegen een prijs van 50-100 $ / kW.
Voor de introductie van brandstofcellen in het dagelijks leven, samen met de goedkopere componenten, moet u nieuwe originele ideeën en benaderingen verwachten. In het bijzonder wordt hoge verwachtingen geassocieerd met het gebruik van nanomaterialen en nanotechnologie. Recent hebben bijvoorbeeld verschillende bedrijven de oprichting aangekondigd van superefficiënte katalysatoren, met name voor een zuurstofelektrode op basis van clusters van nanodeeltjes van verschillende metalen. Bovendien zijn er meldingen geweest van het ontwerp van membraanvrije brandstofcellen waarin vloeibare brandstof (zoals methanol) samen met een oxidatiemiddel aan de brandstofcel wordt geleverd.Een interessant concept is ook het ontwikkelde concept van biobrandstofelementen die in vervuild water werken en opgeloste zuurstof als oxidatiemiddel verbruiken, en organische onzuiverheden als brandstof.
Volgens experts zullen brandstofcellen de komende jaren de massamarkt betreden. Ontwikkelaars overwinnen immers technische problemen na elkaar, rapporteren over successen en presenteren prototypen van brandstofcellen. Toshiba heeft bijvoorbeeld een afgewerkte prototype methanol-brandstofcel aangetoond. Het heeft een afmeting van 22x56x4.5mm en geeft een vermogen in de orde van 100mW. Eén tankbeurt in 2 kubussen geconcentreerde (99,5%) methanol is voldoende voor 20 uur werk van een MP3-speler. Toshiba heeft een commerciële brandstofcel vrijgegeven om mobiele telefoons van stroom te voorzien. Nogmaals, dezelfde Toshiba demonstreerde een element voor het voeden van laptops van 275x75x40mm, waardoor de computer 5 uur kon werken na een enkele tankbeurt.
Een ander Japans bedrijf, Fujitsu, bevindt zich niet ver achter Toshiba. In 2004 introduceerde ze ook een element dat inwerkt op een 30% waterige oplossing van methanol. Deze brandstofcel werkte 10 uur bij één tankbeurt in 300 ml en gaf tegelijkertijd een vermogen van 15 watt.
Casio ontwikkelt een brandstofcel waarin methanol eerst wordt verwerkt tot een mengsel van gasvormig H2 en CO2 in een miniatuurbrandstofconvertor en vervolgens in de brandstofcel wordt ingevoerd. Tijdens de demonstratie leverde het Casio-prototype gedurende 20 uur stroom aan de laptop.
Samsung werd ook genoteerd op het gebied van brandstofcellen - in 2004 demonstreerde het zijn 12 W prototype ontworpen om een laptop van stroom te voorzien. Over het algemeen verwacht Samsung brandstofcellen te gebruiken, vooral in smartphones van de vierde generatie.
Ik moet zeggen dat Japanse bedrijven over het algemeen zeer grondig de ontwikkeling van brandstofcellen hebben benaderd. In 2003 bundelden bedrijven als Canon, Casio, Fujitsu, Hitachi, Sanyo, Sharp, Sony en Toshiba hun krachten om een gemeenschappelijke brandstofcelstandaard voor laptops, mobiele telefoons, PDA's en andere elektronische apparaten te ontwikkelen. Amerikaanse bedrijven, die ook talrijk zijn in deze markt, werken meestal onder contract met het leger en ontwikkelen brandstofcellen voor het opwinden van Amerikaanse soldaten.
De Duitsers lopen niet ver achter - Smart Fuel Cell verkoopt brandstofcellen voor het aansturen van een mobiel kantoor. Het apparaat heet Smart Fuel Cell C25, het heeft afmetingen van 150x112x65mm en kan tot 140 wattuur produceren bij een enkel tankstation. Dit is voldoende om de laptop ongeveer 7 uur van stroom te voorzien. Vervolgens kan de cartridge worden vervangen en kunt u doorgaan met werken. De grootte van de patroon met methanol is 99x63x27 mm en weegt 150 g. Het systeem zelf weegt 1,1 kg, dus je kunt het niet absoluut draagbaar noemen, maar toch is het een compleet en handig apparaat. Het bedrijf ontwikkelt ook een brandstofmodule voor het voeden van professionele videocamera's.
Over het algemeen zijn brandstofcellen bijna op de markt van mobiele elektronica gekomen. Fabrikanten moeten de nieuwste technische problemen oplossen voordat ze met massaproductie beginnen.
Ten eerste is het noodzakelijk om het probleem van miniaturisatie van brandstofcellen op te lossen. Immers, hoe kleiner de brandstofcel, hoe minder vermogen hij kan afgeven - dus worden voortdurend nieuwe katalysatoren en elektroden ontwikkeld die het mogelijk maken om, bij kleine afmetingen, het werkoppervlak te maximaliseren. Hier komen net op tijd de nieuwste ontwikkelingen op het gebied van nanotechnologie en nanomaterialen (bijvoorbeeld nanobuisjes) van pas. Nogmaals, om de leidingen van elementen (brandstof- en waterpompen, koel- en brandstofomzettingssystemen) te miniaturiseren, worden steeds meer micro-elektromechanische vorderingen toegepast.
Het tweede belangrijke probleem dat moet worden aangepakt, is de prijs. Inderdaad, als katalysator in de meeste brandstofcellen wordt zeer kostbaar platina gebruikt.Nogmaals, sommige fabrikanten proberen het beste uit de reeds goed ontwikkelde siliciumtechnologie te halen.
Wat betreft andere gebieden van het gebruik van brandstofcellen, zijn de brandstofcellen daar al goed ingeburgerd, hoewel ze nog niet algemeen zijn geworden in de energiesector of in het vervoer. Reeds veel autofabrikanten hebben hun brandstofcel aangedreven concept cars gepresenteerd. In verschillende steden over de hele wereld rijden brandstofcelbussen rond. Canadian Ballard Power Systems produceert een reeks stationaire generatoren van 1 tot 250 kW. Tegelijkertijd zijn kilowattgenerators ontworpen om één appartement onmiddellijk te voorzien van elektriciteit, warmte en warm water.
Zie ook: Alternatieve energiebronnen
Zie ook op electro-nl.tomathouse.com
:
